Die Mistel in der Tumortherapie
Veröffentlicht am
Update vom 05.02.2025
Naturheilkunde Wissenschaft Krebs
Die Diagnose Krebs erhalten laut Robert Koch-Institut in Deutschland jährlich mehr als 500.000 Menschen; Tendenz steigend auf Grund der Alterung unserer Gesellschaft [01]. Die Therapie ist strapaziös und bedeutet häufig Versehrtheit, Organverluste und zahlreiche Einschränkungen und Belastungen. In dieser Situation möchten zahlreiche Patient*innen selbst etwas tun, selbst Initiative ergreifen, etwas zu ihrer Gesundung beitragen und sind daher auf der Suche nach ergänzenden, komplementären Angeboten. Ein großer Teil der Bevölkerung in Deutschland nimmt diese Angebote in Anspruch.
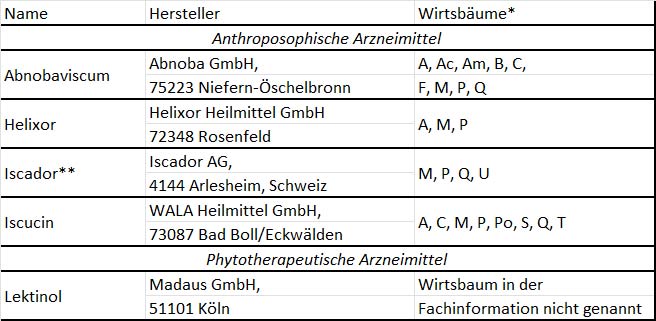
In Deutschland gibt es Mistelpräparate von fünf Herstellern, vier davon aus der anthroposophischen Medizin, einer aus der Pflanzenheilkunde (Phytotherapie).
MehrDie Wirkungen von Mistelpräparaten sind durch vielfältige therapeutische Erfahrung und zahlreiche klinische Studien bestätigt. Es gibt zahlreiche Reviews zur Beurteilung der klinischen Wirksamkeit. Leider sind diese von unterschiedlicher Qualität und zum Teil geprägt durch die Auseinandersetzung zwischen Vertretern der konventionellen und der komplementären Medizin.
MehrDie Misteln werden zu unterschiedlichen Jahreszeiten geerntet, überwiegend in Wildsammlung. Bei ausgewählten Wirtsbäumen erfolgt die Ernte auch aus Standorten mit kultivierten Misteln. Bei der Eiche und der Ulme gibt es sie bereits, bei der Esche und beim Apfelbaum werden sie gerade angelegt.
MehrHäufig beschrieben sind für die Mistel als auch ihre wässrigen Extrakte Inhaltsstoffe wie Mistellektine, Viscotoxine, Flavonoide, Poly- und Oligosaccharide, Jasmonate und viele andere mehr, auch Triterpene, fettlösliche Substanzen, die in den wässrigen Extrakten nur in geringem Umfang zu finden sind.
MehrTypisch ist beispielsweise die regelmäßige, gleichwertig gabelige (dichotome) Verzweigung der grünen Stängel. An ihrer Spitze entwickeln sich in jedem Jahr eine Knospe oder ein Wirtel mit 2-5 sehr kleinen, unscheinbar wirkenden Blüten und zwei gegenüberliegende (kreuzgegenständig angeordnete) zungenförmige, glattrandige, grün bis gelbgrüne, beidseitig gleichausgebildete, ungestielte Laubblätter. Bis zum Juni werden die Blätter ohne weitere Gestaltveränderung nur noch etwas größer. Auch die Stängel wachsen; sie sind zunächst flexibel und verholzen in der Folge spät und wenig, ohne wie ihre Wirte totes Abschlussgewebe zu bilden. Im Gegensatz zu den Laubblättern bei anderen Pflanzen sind bei den Blättern der Mistel Blattunter- und Oberseite gleich ausgebildet. Sie fallen bei den Laubholzmisteln erst nach 2 Jahren ab, ohne zu welken.
MehrSprungmarken innerhalb des Artikels:
- Einleitung
- Die Mistel – eine besondere Pflanze
- Über die Inhaltsstoffe der Mistel und ihre Wirkungen
- Mistelpräparate in Deutschland, Grundzüge ihrer Herstellung
- Wie werden Mistelpräparate in der Behandlung von krebskranken Menschen angewendet und welche Reaktionen treten auf?
- Zur Wirksamkeit der Mistel: Die Mistel in der klinischen Anwendung, in Studien und ihre Bewertung
- Zukünftige Entwicklungen in der Misteltherapie
- Literatur
Einleitung
Eine Brücke zur Schulmedizin ist die sog. Integrative Onkologie [02], die im Sinne einer bestmöglichen Versorgung der Patient*innen komplementärmedizinische Behandlungen ergänzend zur konventionellen Onkologie (Schulmedizin) zur Anwendung bringt. Sie ist ein sinnvolles Gesamtkonzept, das den ganzen Menschen und die therapeutische Beziehung zwischen Arzt bzw. Therapeut und Patient umfasst. Im Rahmen einer solchen ganzheitlichen Krebsbehandlung, die neben der konventionellen Onkologie beispielsweise psychisch stützende Verfahren, Ernährungs-, Bewegungs-, künstlerische und Pflege-Therapien umfasst, wird neben unterschiedlichen Begleitmedikamenten auch die Mistel eingesetzt. Wie dann die Behandlung im Detail aussieht, ist individuell unterschiedlich und wird je nach Erkrankung und daraus resultierendem Bedarf gemeinsam mit den Patient*innen festgelegt. Seit Mitte 2021 gibt es eine S3 Leitlinie [Anmerkung 1] zur Komplementärmedizin in der Krebstherapie, die diesen integrativen Ansatz in der Onkologie unterstützen soll [03, 04].
[Anmerkung 1]
S3 Leitlinie: Leitlinien geben Empfehlungen, wie eine Erkrankung festgestellt und behandelt werden sollte. Bei einer S3-Leitlinie hat eine repräsentativ zusammengesetzte Kommission das Wissen dazu systematisch gesammelt und bewertet.
Die Onkologie im Wandel und Hoffnung auf weitere Verbesserungen
Hinzu kommt der rasante Wandel, in dem die gesamte Onkologie begriffen ist. Es gibt neue erfolgreiche Therapien, beispielsweise die sog. neuen immunologischen Therapien (z.B. Checkpoint Inhibitoren), die neue Hoffnungen auf weitere Verbesserungen wecken. In dem Maße, wie sich die Onkologie wandelt, wird sich, ja muss sich auch der Beitrag der Misteltherapie weiter entwickeln und seinen Platz jeweils neu bestimmen.
Die Aufgabe der Mistelsymposien
Hier haben die sog. Mistelsymposien [05] ihre Aufgabe, die seit annähernd drei Jahrzehnten von verschiedenen pharmazeutischen und medizinischen Fachgesellschaften veranstaltet werden. Die vom Autor dieses Artikels zusammen mit einem Kollegium von Wissenschaftler*innen und Ärzt*innen organisierten Veranstaltungen werden u.a. von der Karl und Veronica Carstens-Stiftung gefördert. Alle vier Jahre kommen Fachleute aus Biologie, Pharmazie und Medizin und damit verwandten Wissenschaftsbereichen zusammen, um Aktuelles aus Forschung und Klinik der Mistel in der Tumortherapie zu präsentieren und miteinander zu diskutieren. Dadurch soll ein umfassendes Bild vom Stand der wissenschaftlichen Erkenntnisse ermöglicht werden. In einer solchen wissenschaftlichen Diskussion kann die Anwendung von Mistelpräparaten zum Wohle der Patient*innen weiterentwickelt werden, lassen sich Möglichkeiten und Grenzen der Misteltherapie besser erkennen. Dieser interdisziplinäre Dialog fand zuletzt mit dem 8. Mistelsymposium in der Europäischen Akademie Otzenhausen in Nonnweiler (Saarland) vom 9. – 11. November 2023 statt [5.1] und soll mit dem 9. Mistelsymposium 2027 fortgesetzt werden.
Sämtliche Abstracts des 8. Mistelsymposiums sind in einem Sonderband des Journal of Integrative and Complementary Medicine veröffentlicht und bis Oktober 2026 frei zugänglich [5.2]. Die ausführlichen Beiträge wurden im November 2024 in einem Tagungsband veröffentlicht [5.3]. Videomitschnitte einer innerhalb des Symposiums eingebundenen ärztlichen Fortbildung zur „Praxis der Misteltherapie“ stehen zur Ansicht auf der Symposiums-Homepage zur freien Verfügung [5]. Der Zugang erfolgt über DocCheck.
Die Mistel – eine besondere Pflanze
Wenn man von Misteln spricht, ist zumeist nur eine Art, nämlich die heimische Weißbeerige Mistel mit dem wissenschaftlichen Namen Viscum album L. [Anmerkung 2] gemeint und meistens nicht die Gesamtheit der halbparasitär auf Bäumen und Sträuchern wachsenden weit über 100 Viscum-Arten, die überwiegend in den Tropen vorkommen [06]. „Unsere Mistel“ gehört zur Familie der Sandelholzgewächse (Santalaceae), ist Licht- und Wärme-liebend und an unser Klima angepasst. Über ihren Senker ist sie tief im Holz der Wirtspflanze verankert, mit deren Wasserleitgewebe, dem Xylem, verbunden. Von dort bezieht sie zumeist anorganische Nährstoffe und große Mengen Wasser. Aber auch der Zustrom von stickstoffhaltigen organischen Substanzen wie Aminosäuren lässt sich nachweisen, und über eine Verbindung zum Phloem, der Nährstoffleitung des Wirtes, wird diskutiert. Als Halbparasit verfügt die Mistel über eigenes Blattgrün (Chlorophyll) – von den Blättern über die Stängel bis zum Senker - und ist dadurch selbst zur Photosynthese, das heißt Energiegewinnung und Bildung Mistel-eigener Substanzen (Mistellektine, Viscotoxine; siehe später) befähigt.
[Anmerkung 2]
Das L. ist das offizielle botanische Autorenkürzel des schwedischen Naturforschers Carl von Linné (1707-1778), der diese Art wissenschaftlicher Namensgebung entwickelte, sowie den Namen Viscum album erstveröffentlicht hat.
Häufig sehen wir sie im Winter hoch oben in den Kronen der zu diesem Zeitpunkt unbelaubten Bäume, grün-gelbliches Laub tragende kugelförmige Büsche mit bis zu 1,4 Meter Durchmesser, häufig auf Pappeln, Weiden, Linden, Apfelbäumen und zahlreichen anderen Laubbäumen, aber auch auf Sträuchern wie Weißdorn. Für die Arzneimittelherstellung werden neben dieser Unterart (Laubholzmistel: V. album subspecies album) die in Mitteleuropa außerdem vorkommenden Unterarten Tannen- (V. album subsp. abietis) und Kiefernmistel (V. album subsp. austriacum) verwendet. Es gibt auch Bäume, auf denen Misteln sehr selten (Eiche) oder gar nicht (Buche) wachsen. In jüngster Zeit wird ein zunehmender Mistelbefall durch beispielsweise Klimawandel und fehlende Baumpflege auf Streuobstwiesen beobachtet [07]. In trockenen Jahren, wie wir sie zuletzt hatten, und auf Grund der durch die Mistel verursachten hohen Wasserverdunstung geraten die Wirtspflanzen in Trockenstress und sind dann empfänglich für Krankheiten, bzw. wenn die Mistel auf einem Baum in Massen auftritt, bringt sie ihn zum Absterben. Die Mistel kann bis zu 70 Jahre alt werden [08]. Zu ihrer Verbreitung, entweder durch Vögel wie Mönchsgrasmücke, Drossel und andere Singvögel, trägt ganz wesentlich die Klebrigkeit ihrer Samen bei (dazu siehe später).
Nach Ausscheidung der unverdauten Samen oder durch Abstreifen der am Gefieder oder Schnabel klebenden Beeren oder Samen am Ast oder Stamm ist der Kontakt zur Wirtspflanze, die auch eine andere Mistel sein kann, hergestellt. Auch eine Vogel-unabhängige Verbreitung durch bis zu 20 cm lange, schnurförmig zusammenhängende Samen-Ketten ist beschrieben [07], entweder innerhalb des befallenen Baumes oder bei stärkerem Wind auch auf andere Bäume. Zunächst bildet der Keimling eine Haftscheibe, ein Haustorium, aus, um von dort durch die Rinde einzudringen und sich mittels eines zapfenartigen Senkers mit dem Wasserleitgewebe der Wirtspflanze zu verbinden. Das ist, wie für die Mistel typisch, ein langsamer Prozess. Es dauert ca. ein halbes Jahr, bis das erste Blattpaar der jungen Pflanze erscheint. Dann ist sie angewachsen, was sich auch am Anschwellen des Querschnitts der Wirtspflanze an der Haftstelle zeigt.